EFE/@pfizerinc
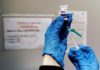
La compañía farmacéutica Pfizer y su socia alemana BioNTech anunciaron que solicitarán este viernes una autorización de emergencia a la Administración de Alimentos y Fármacos de Estados Unidos (FDA) para su vacuna contra la covid-19.
Esta es la primera vacuna contra el coronavirus que busca una autorización del organismo regulador de Estados Unidos y que podría estar disponible a mediados o finales de diciembre para grupos de riesgo, según indicó la compañía en un comunicado.
Además de la presentación de hoy a la FDA, las empresas aún no han iniciado presentaciones continuas en todo el mundo, incluidos Australia, Canadá, Europa, Japón y el Reino Unido, y planean enviar solicitudes de inmediato a otras agencias reguladoras de todo el mundo.
Según las proyecciones actuales, las empresas esperan producir a nivel mundial hasta 50 millones de dosis en 2020 y hasta 1.300 millones de dosis para fines de 2021; las empresas estarán listas para distribuir la vacuna pocas horas después de la autorización.
BNT162b2 demostró una tasa de eficacia de la vacuna del 95%, sin que se hayan observado problemas de seguridad graves hasta la fecha.